文章来源:赢享分子诊断公众号(ID: daangenescb)
近日,达安基因最新研制的结核分枝杆菌复合群核酸检测试剂盒(PCR-荧光探针法)取得国家药品监督管理局(NMPA)三类医疗器械认证,注册证号:国械注准20223401618。


性能优异
最低检出限为1个菌/mL。
全面精准
结核分枝杆菌、牛分枝杆菌和非洲分枝杆菌均能引起人类患病且症状相似,复合群的检测有助于各病原体精准检出,避免漏检。
安全可靠
外源性内标及UNG酶,避免假阴性及假阳性。
多样本覆盖
可对痰液样本、支气管肺泡灌洗液样本检测。
自动快速
搭配磁珠法核酸提取试剂,实现自动化、高通量便捷操作。
便捷操作
单管单人份试剂,无需配液,加样即检。

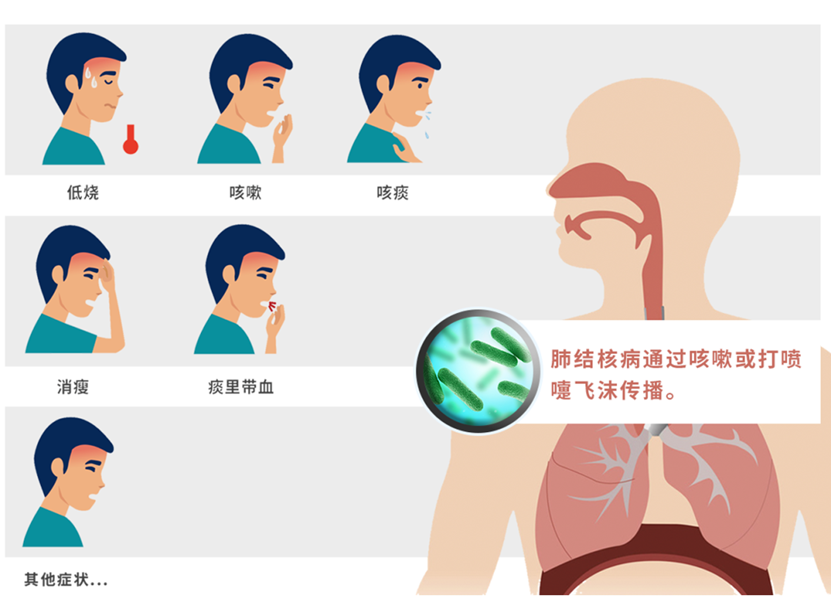
结核病是一种慢性传染疾病,由结核分枝杆菌复合群引起,通过呼吸道飞沫和尘埃传播,以肺部结核感染最为常见,非肺部的结核感染则称为肺外结核。人体感染结核菌后不一定发病,当抵抗力降低或细胞介导的变态反应增高时,可能引起临床发病,患者一般出现食欲减退、疲劳,胸痛、咳嗽、咳血,盗汗、脸色苍白等症状。
我国结核病防控形势严峻,据WHO发布的2022全球结核病报告估计,2021年我国新发感染人数约78万,居全球第三位。因此,对结核病患者和新近感染者进行精准诊断,将结核预防、筛查、诊治关口前移,对终止全球结核病流行至关重要。


结核分枝杆菌复合群主要包括结核分枝杆菌(M.tuberculosis)、牛分枝杆菌(M.bovis)、非洲分枝杆菌(M.africanum)和田鼠分枝杆菌(M.microti)。其中结核分枝杆菌、牛分枝杆菌和非洲分枝杆菌均能引起人类患病,三者所引起的结核病症状相似。
结核分枝杆菌
人类感染的结核主要由结核分枝杆菌所致。结核分枝杆菌是人类结核病的主要病原株,其造成的结核病至今仍位列全球第十三大死亡原因。
牛分枝杆菌
在人的结核病例中约有5%~10%由牛分枝杆菌感染引起。WHO估计2019年全球因感染牛分枝杆菌而引起的结核病共有14万例,死亡11400例。
非洲分枝杆菌
非洲分枝杆菌在一般人群中的流行率较低,而在非洲多达半数的结核病例均由此病原菌感染所致。
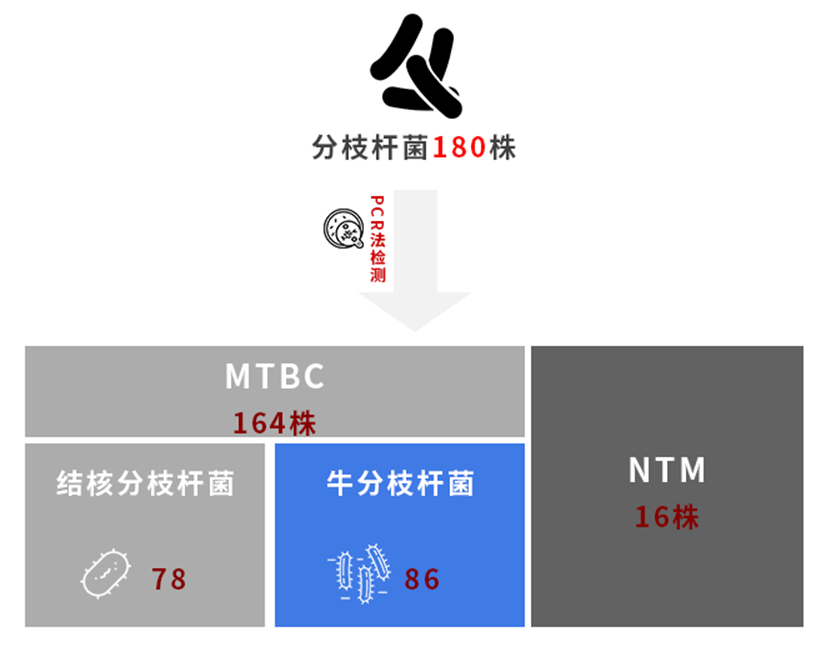
有文献研究数据表示,在上海市某医院结核患者中,对180株分枝杆菌阳性培养物进行PCR法检测,其中16株为非结核分枝杆菌,164株为结核分枝杆菌复合群。对结核分枝杆菌复合群进行特异性分析,其中78株为结核分枝杆菌,剩余86株为牛分枝杆菌。可见,牛分枝杆菌在结核患者中也有较高的比例,不容忽视。
世界卫生组织在消除结核病策略中,强调病原学诊断的重要性及早期诊断的必要性,以减少重症结核病的发生。目前,结核病患者的病原学阳性率整体偏低,不足60%,因此,行业亟需能提高肺结核患者病原学检出率的检测技术及相关产品,尽早发现肺结核患者,避免其对周边人群的传播。
《肺结核诊断标准WS288-2017》
由于分子检测具有高灵敏度、高特异性等特点,诊断标准增加了分子生物学检查,检测出MTBC核酸可作为确诊证据。
《病原学检测阴性肺结核诊断流程(T/CHATA 008—2020)》
实验室检查:要求必须对所有就诊患者开展包括涂片、培养和分子生物学等病原学检测。对于无痰或未能留取合格痰标本的患者,可采用痰诱导技术帮助患者留痰或行纤维支气管镜采集支气管肺泡灌洗液,均能提高病原学检测阳性率。
《“十四五”国民健康规划》
全面落实结核病防治策略,加强肺结核患者发现和规范化诊疗,实施耐药高危人群筛查,强化基层医疗卫生机构结核病患者健康管理,加大肺结核患者保障力度。
结核复合群核酸检测试剂盒不仅能检测引起结核病的结核分枝杆菌,还能检测牛结核分枝杆菌、非洲分枝杆菌等引起人类结核的病原体,此外,荧光PCR法具有高灵敏度、高特异性等特点,相比于培养、染色法等,具备更高的阳性检出率,因此,基于PCR技术开发的结核杆菌复合群核酸检测试剂,可提高结核病原学阳性检出率,有助于快速、全面发现病原菌,为临床决策提供更面的依据。
达安基因深耕于传染性疾病诊断细分领域,持续提升产品力与方案力。目前,达安基因结核检测整体方案涵盖结核诊断、结核耐药筛查等流程,产品包括结核分枝杆菌核酸检测、结核分枝杆菌复合群核酸检测、结核分枝杆菌异烟肼耐药突变基因检测以及结核分枝杆菌利福平耐药突变基因检测。达安基因结核检测整体方案助力提高结核病原学阳性率,指导临床治疗,早日实现“无核”社会!
参考文献:
[1] 世界卫生组织2022年全球结核报告
[2] JOURNAL OF CLINICAL MICROBIOLOGY, Nov. 2011, p. 3837–38410095-1137/11/$12.00 doi:10.1128/JCM.01172-11
[3] De Jong, B. C., Antonio, M., & Gagneux, S. (2010). Mycobacterium africanum—Review of an Important Cause of Human Tuberculosis in West Africa. PLoS Neglected Tropical Diseases, 4(9), e744. doi:10.1371/journal.pntd.0000744
[4] Sun YS, Lou SQ, Wen JM, Lv WX, Jiao CG, Yang SM, Xu HB. Clinical value of polymerase chain reaction in the diagnosis of joint tuberculosis by detecting the DNA of Mycobacterium tuberculosis. Orthop Surg. 2011 Feb;3(1):64-71. doi: 10.1111/j.1757-7861.2010.00115.x. PMID: 22009983; PMCID: PMC6583303.
[5] Sharma, A., Bloss, E., Heilig, C. M., & Click, E. S. (2016). Tuberculosis Caused by Mycobacterium africanum, United States, 2004–2013. Emerging Infectious Diseases, 22(3), 396–403. doi:10.3201/eid2203.151505
[6] 邓桂林. 上海市某医院儿童结核病流行现况及结核分枝杆菌复合群分子生物学特征研究[D]. 复旦大学.
近日,达安基因最新研制的结核分枝杆菌复合群核酸检测试剂盒(PCR-荧光探针法)取得国家药品监督管理局(NMPA)三类医疗器械认证,注册证号:国械注准20223401618。


性能优异
最低检出限为1个菌/mL。
全面精准
结核分枝杆菌、牛分枝杆菌和非洲分枝杆菌均能引起人类患病且症状相似,复合群的检测有助于各病原体精准检出,避免漏检。
安全可靠
外源性内标及UNG酶,避免假阴性及假阳性。
多样本覆盖
可对痰液样本、支气管肺泡灌洗液样本检测。
自动快速
搭配磁珠法核酸提取试剂,实现自动化、高通量便捷操作。
便捷操作
单管单人份试剂,无需配液,加样即检。

结核病是一种慢性传染疾病,由结核分枝杆菌复合群引起,通过呼吸道飞沫和尘埃传播,以肺部结核感染最为常见,非肺部的结核感染则称为肺外结核。人体感染结核菌后不一定发病,当抵抗力降低或细胞介导的变态反应增高时,可能引起临床发病,患者一般出现食欲减退、疲劳,胸痛、咳嗽、咳血,盗汗、脸色苍白等症状。

我国结核病防控形势严峻,据WHO发布的2022全球结核病报告估计,2021年我国新发感染人数约78万,居全球第三位。因此,对结核病患者和新近感染者进行精准诊断,将结核预防、筛查、诊治关口前移,对终止全球结核病流行至关重要。


结核分枝杆菌复合群主要包括结核分枝杆菌(M.tuberculosis)、牛分枝杆菌(M.bovis)、非洲分枝杆菌(M.africanum)和田鼠分枝杆菌(M.microti)。其中结核分枝杆菌、牛分枝杆菌和非洲分枝杆菌均能引起人类患病,三者所引起的结核病症状相似。
结核分枝杆菌
人类感染的结核主要由结核分枝杆菌所致。结核分枝杆菌是人类结核病的主要病原株,其造成的结核病至今仍位列全球第十三大死亡原因。
牛分枝杆菌
在人的结核病例中约有5%~10%由牛分枝杆菌感染引起。WHO估计2019年全球因感染牛分枝杆菌而引起的结核病共有14万例,死亡11400例。
非洲分枝杆菌
非洲分枝杆菌在一般人群中的流行率较低,而在非洲多达半数的结核病例均由此病原菌感染所致。
有文献研究数据表示,在上海市某医院结核患者中,对180株分枝杆菌阳性培养物进行PCR法检测,其中16株为非结核分枝杆菌,164株为结核分枝杆菌复合群。对结核分枝杆菌复合群进行特异性分析,其中78株为结核分枝杆菌,剩余86株为牛分枝杆菌。可见,牛分枝杆菌在结核患者中也有较高的比例,不容忽视。

世界卫生组织在消除结核病策略中,强调病原学诊断的重要性及早期诊断的必要性,以减少重症结核病的发生。目前,结核病患者的病原学阳性率整体偏低,不足60%,因此,行业亟需能提高肺结核患者病原学检出率的检测技术及相关产品,尽早发现肺结核患者,避免其对周边人群的传播。

《肺结核诊断标准WS288-2017》
由于分子检测具有高灵敏度、高特异性等特点,诊断标准增加了分子生物学检查,检测出MTBC核酸可作为确诊证据。
《病原学检测阴性肺结核诊断流程(T/CHATA 008—2020)》
实验室检查:要求必须对所有就诊患者开展包括涂片、培养和分子生物学等病原学检测。对于无痰或未能留取合格痰标本的患者,可采用痰诱导技术帮助患者留痰或行纤维支气管镜采集支气管肺泡灌洗液,均能提高病原学检测阳性率。
《“十四五”国民健康规划》
全面落实结核病防治策略,加强肺结核患者发现和规范化诊疗,实施耐药高危人群筛查,强化基层医疗卫生机构结核病患者健康管理,加大肺结核患者保障力度。
结核复合群核酸检测试剂盒不仅能检测引起结核病的结核分枝杆菌,还能检测牛结核分枝杆菌、非洲分枝杆菌等引起人类结核的病原体,此外,荧光PCR法具有高灵敏度、高特异性等特点,相比于培养、染色法等,具备更高的阳性检出率,因此,基于PCR技术开发的结核杆菌复合群核酸检测试剂,可提高结核病原学阳性检出率,有助于快速、全面发现病原菌,为临床决策提供更面的依据。
达安基因深耕于传染性疾病诊断细分领域,持续提升产品力与方案力。目前,达安基因结核检测整体方案涵盖结核诊断、结核耐药筛查等流程,产品包括结核分枝杆菌核酸检测、结核分枝杆菌复合群核酸检测、结核分枝杆菌异烟肼耐药突变基因检测以及结核分枝杆菌利福平耐药突变基因检测。达安基因结核检测整体方案助力提高结核病原学阳性率,指导临床治疗,早日实现“无核”社会!
参考文献:
[1] 世界卫生组织2022年全球结核报告
[2] JOURNAL OF CLINICAL MICROBIOLOGY, Nov. 2011, p. 3837–38410095-1137/11/$12.00 doi:10.1128/JCM.01172-11
[3] De Jong, B. C., Antonio, M., & Gagneux, S. (2010). Mycobacterium africanum—Review of an Important Cause of Human Tuberculosis in West Africa. PLoS Neglected Tropical Diseases, 4(9), e744. doi:10.1371/journal.pntd.0000744
[4] Sun YS, Lou SQ, Wen JM, Lv WX, Jiao CG, Yang SM, Xu HB. Clinical value of polymerase chain reaction in the diagnosis of joint tuberculosis by detecting the DNA of Mycobacterium tuberculosis. Orthop Surg. 2011 Feb;3(1):64-71. doi: 10.1111/j.1757-7861.2010.00115.x. PMID: 22009983; PMCID: PMC6583303.
[5] Sharma, A., Bloss, E., Heilig, C. M., & Click, E. S. (2016). Tuberculosis Caused by Mycobacterium africanum, United States, 2004–2013. Emerging Infectious Diseases, 22(3), 396–403. doi:10.3201/eid2203.151505
[6] 邓桂林. 上海市某医院儿童结核病流行现况及结核分枝杆菌复合群分子生物学特征研究[D]. 复旦大学.



